Parallèlement au développement de nouveaux traceurs pour l’imagerie TEP, notre équipe s’intéresse à la mise au point de méthodes innovantes pour le marquage au fluor-18 et au carbone-11 de différentes structures, des molécules organiques simples aux macromolécules biologiques.
Méthodologie de marquage au Carbone-11
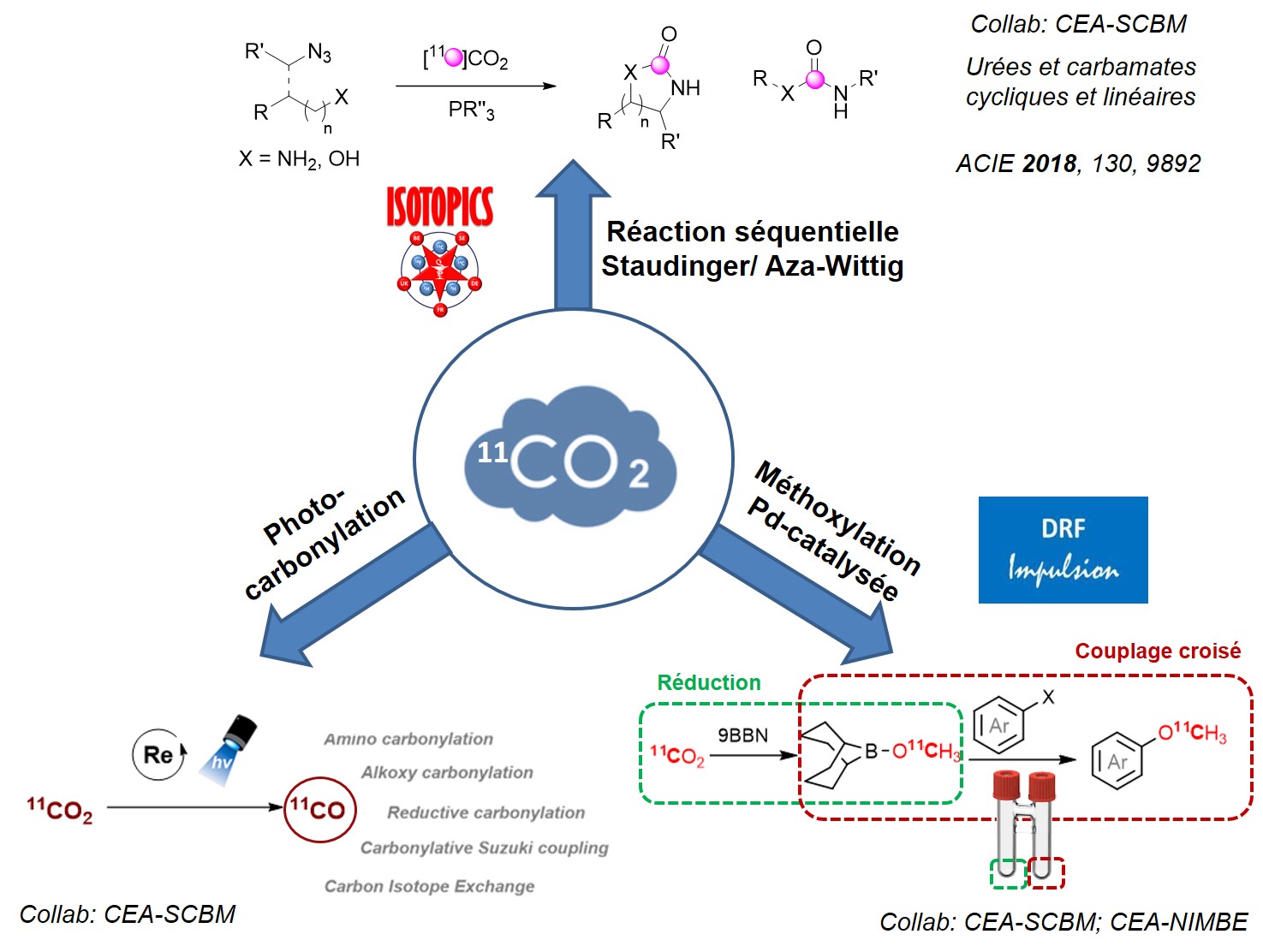
Les techniques de radiomarquage au carbone-11 reposent dans plus de 95% des cas sur des approches de méthylation d’hétéroatomes, limitant la variété de traceurs disponibles pour l’imagerie TEP. De plus, la source primaire de carbone-11, le dioxyde de carbone [11C]CO2 produit en cyclotron, doit être transformée en agent méthylant ([11C]CH3I ou [11C]CH3OTf) selon des processus multi-étapes longs en regard de la demi-vie de carbone-11 (t1/2 = 20.4 minutes) et limitantes pour les rendements de production en radiotraceur. Nous développons donc de nouvelles méthodes de marquage au carbone-11 innovantes et orthogonales permettant d’incorporer directement le [11C]CO2 au sein de motifs moléculaires complexes pour i) accélérer les processus de radiomarquage et ainsi augmenter les rendements de production ii) élargir l’éventail des fonctions chimiques marquées au carbone-11 et donc le panel de radiotraceurs accessibles [1].
Méthodologie de marquage au Fluor-18
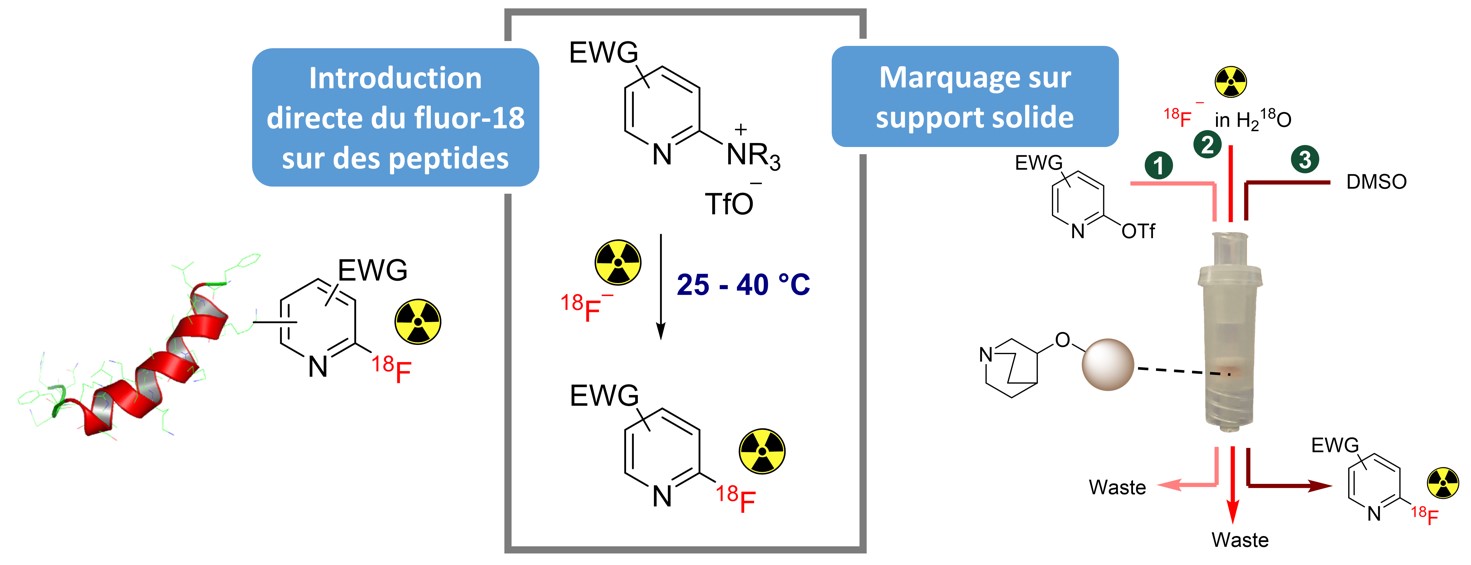
Certains hétérocycles tels que les pyridines possèdent une réactivité intéressante pour des réactions de substitution nucléophile aromatique, qui sont particulièrement favorisées sur ce noyau. Nous avons démontré qu’un appauvrissement de la densité électronique des pyridines permettait de réaliser leur marquage avec du fluor-18 à des températures bien plus basses que celles habituellement décrites pour cette réaction. Ceci nous a permis de développer plusieurs applications telles que le marquage direct de peptides ou le marquage sur support solide [2].
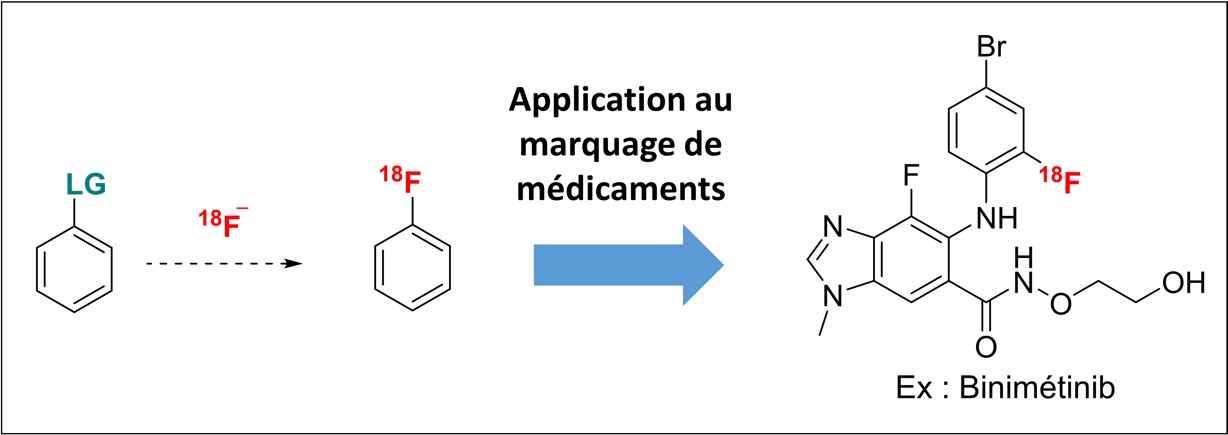
Nous étudions également de nouvelles approches pour la radiofluoration aromatique faisant intervenir des substrats originaux et hautement réactifs pour compenser la faible réactivité de l’ion [18F]fluorure, dans le but de les appliquer à des substrats d’intérêt thérapeutique particulièrement difficiles à marquer.
Marquage d’objets biologiques complexes (des peptides aux protéines) au Fluor-18
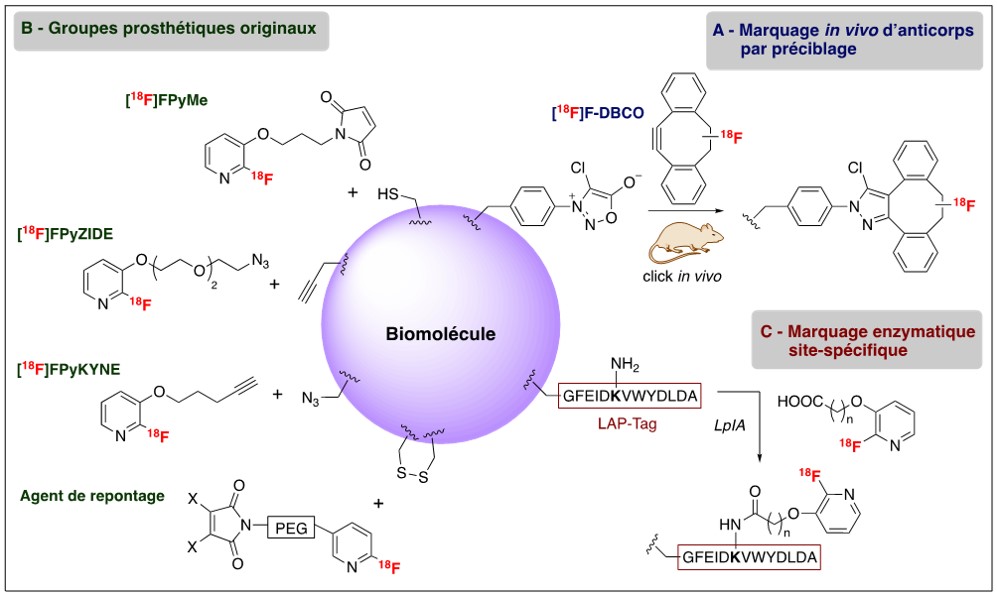
Notre équipe développe diverses méthodes pour le radiomarquage de biomolécules :
-
- Réaction de SPSAC bioorthogonale entre une biomolécule conjuguée à une sydnone et un alcyne contraint radiomarqué (18F-DBCO, A). Cette réaction a été mise en application pour le marquage in vivo par préciblage d’un anticorps ciblant les récepteurs EGFR [3].
- Développement de différents groupes prosthétiques (B), parmi lesquels :
FpyZIDE [4]
FPyMe [5]
FPyKYNE [6]
Un agent de repontage de ponts disulfures
Marquage enzymatique spécifique de protéines avec une haute activité molaire (LAP-Tag, C)
Conception de sondes multimodales et multivalentes
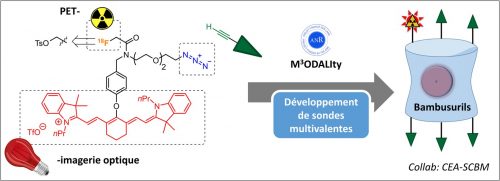
L’un des projets développés dans l’équipe concerne la mise au point de sondes bimodales pour une application en imagerie TEP et imagerie de fluorescence. Dans cette optique, une molécule présentant une cyanine et un précurseur de radiofluoration a été préparé et radiomarqué. Grâce à la présence d’un azoture, la sonde bimodale peut ensuite être couplée à un vecteur de ciblage. Cet objet est également utilisé pour la conception de sondes multivalentes, possédant plusieurs entités de ciblages sur une même plateforme.
Références
[1] Del Vecchio A, Caille F, Chevalier A, Loreau O, Horkka K, Halldin C, Schou M, Camus N, Kessler P, Kuhnast B, Taran F, Audisio D. Late-Stage Isotopic Carbon Labeling of Pharmaceutically Relevant Cyclic Ureas Directly from CO2. (2018), Angewandt Chemie, 57, 9744-9748, doi : 10.1002/anie.201804838.
[2] Richard M , Specklin S , Roche M , Hinnen F , Kuhnast B. Original synthesis of radiolabeling precursors for batch and on resin one-step/late-stage radiofluorination of peptides. (2020), Chem Commun, 56, 2507-2510, doi: 10.1039/c9cc09434b
[3] Richard M , Truillet C , Tran VL , Liu H , Porte K , Audisio D , Roche M , Jego B , Cholet S , Fenaille F , Kuhnast B , Taran F , Specklin S. New fluorine-18 pretargeting PET imaging by bioorthogonal chlorosydnone-cycloalkyne click reaction. (2019), Chem Commun, 55, 10400-10403, doi: 10.1039/c9cc05486c.
[4] Roche M, Specklin S, Richard M, Hinnen F, Générmont K, Kuhnast B. [18F]FPyZIDE : a versatile prosthetic reagent for the fluorine-18 radiolabeling of biologics via copper-catalyzed or strained-promoted alkyne-azide cycloadditions. (2018), J Label Compds Radiopharm, 62, 95-108, doi: 10.1002/jlcr.3701.
[5] de Bruin B, Kuhnast B, Hinnen F, Yaouancq L, Amessou M, Johannes L, Samson A, Boisgard R, Tavitian B, Dollé F. 1-[3-(2-[18F]fluoropyridin-3-yloxy)propyl]pyrrole-2,5-dione: design, synthesis, and radiosynthesis of a new [18F]fluoropyridine-based maleimide reagent for the labeling of peptides and proteins. (2005), Bioconjug Chem, 16, 406-20, doi: 10.1021/bc0497463.
[6] Kuhnast B, Hinnen F, Tavitian B, Dollé F. [18F]FPyKYNE, a fluoropyridine‐based alkyne reagent designed for the fluorine‐18 labelling of macromolecules using click chemistry. (2008), J Label Compds Radiopharm, 51, 336-342, doi.org/10.1002/jlcr.1533.